Propiedades de los Solventes usados en HPLC
 Los solventes en HPLC se utilizan como:
Los solventes en HPLC se utilizan como:
- Fases Móviles
- Para disolver la muestra
- Para preparar las muestras
El uso como Fases Móviles es de principal importancia puesto que sus propiedades han de mantenerse en límites estrechos de aceptabilidad. Además esas propiedades también influyen en la elección del solvente de disolución y el de preparación de la muestra.
En la TABLA 1, se muestran varias propiedades que son importantes al seleccionar el o los solventes en una aplicación de HPLC.

La elección final del solvente más adecuado se basará en los siguientes principios básicos:
- Compatibilidad con el detector
- Polaridad y Selectividad
- Seguridad
1. Compatibilidad con la Detección
1.1. Detección UV
La fase móvil debería tener una absorbancia A < 0.2 AU en la longitud de onda seleccionada para la detección de la muestra: una menor absorbancia permite una mayor precisión del ensayo y mejores resultados en condiciones de elución por gradiente, aunque una absorbancia mayor puede resultar aceptable en algunas separaciones isocráticas.
La TABLA 2 resume las absorbancias de los solventes más usados en CFI (RPC) entre 200 y 260 nm. Raramente se usan longitudes de onda <200 nm, excepto en casos muy concretos de solutos con baja absorbancia (carbohidratos, triglicéridos, ácidos grasos…)

Puesto que el agua no absorbe a 200 nm o por encima, la absorbancia de las fases móviles con agua será la misma que la del solvente puro multiplicada por la fracción de volumen (f) del solvente B. Por ejemplo a 220 nm fases móviles con un 25% de los solventes listados de la Tabla 2 tendrán absorbancias de: Acetonitrilo 0.00 AU, Metanol 0.06 AU, THF 0.17 AU, IPA 0.05 AU.
La desgasificación contribuye a una menor absorbancia (aproximadamente un 30% menor) entre 200 y 240 nm en función del menor contenido de oxígeno disuelto, que es mayor cuanto más polar sea el solvente: el efecto de la desgasificación será más notable en solventes más polares como el THF o el IPA.
Se asume que el agua ha sido purificada según ASTM D1139 y que además, si se requieren niveles de detección muy bajos, el valor de TOC (Total Organic Carbon) ha de ser < 50 ppb y la resistividad alta.
En la TABLA 3 se muestran los valores UV de cutoff para varios solventes.

En condiciones de gradiente es necesario que la respuesta del detector se mantenga constante, y es necesario que el solvente A (normalmente agua) y el solvente B respondan de manera similar y si se trabaja a bajas longitudes de onda la elección de solventes disponibles se reduce considerablemente.
1.2. Detección por Índice de Refracción
En condiciones isocraticas la selección de eluyentes no resulta crítica y la sensibilidad puede incrementarse con fases móviles cuyo Índice de Refracción (IR) sea lo más diferente posible que el de los componentes de la mezcla (ver TABLA 3).
Los detectores de IR no pueden utilizarse en condiciones de gradiente por la gran diferencia de respuesta que pueden tener el solvente A y B.
1.3. Detección MS
La interfase de un Espectrómetro de Masas evapora la fase móvil. Las fases móviles como agua, solventes orgánicos y aditivos han de ser volátiles y han de evitarse sales o tapones no volátiles.
Al eliminarse la fase móvil su absorción UV o Índice de Refracción no son factores limitantes pero los solventes han de estar libres de partículas.
2. Polaridad y Selectividad
En la TABLA 4 se muestran los propiedades de los solventes que afecta a la fuerza, selectividad y solubilidad. La «Selectividad Normalizada» incluye tres contribuciones a la interacción soluto.solvente: La Acidez y la Basicidad de Enlace de Hidrógeno y la Dipolaridad.

Estos tres parámetros son la base del triángulo de la selectividad:

Otro triangulo muy popular en cromatografia FLASH y Fase Normal es el siguiente (vea como aplicarlo AQUÍ:

La TABLA 4 muestra el valor de P’, una medida de la polaridad media del solvente. La solubilidad de la muestra tiene relación con los valores de P’ (lo similar disuelve lo similar). Las muestras tienden a ser más solubles en solventes de P’ similar. Los solventes menos polares como los hidrocarburos disolverán muestras poco polares (valor de P’ bajo). Al contrario solventes con alto P’, disolverán muestra más polares.
La constante dieléctrica ε también tiene relación con la habilidad del solvente de disolver solutos ionizados o tampones: un valor alto de ε favorece la solubilización de compuestos ionizables.
La TABLA 5 muestra valores de viscosidad de mezclas MeOH/Agua y ACN/Agua en función de la temperatura.

Los datos mostrados pueden usarse para estimar la pérdida de carga según la ecuación:
Donde L es la longitud de la columna en mm, η es la viscosidad en cp, F el caudal en mL/min, dc es el diámetro interno de la columna y dp es el diámetro de la partícula en µm.
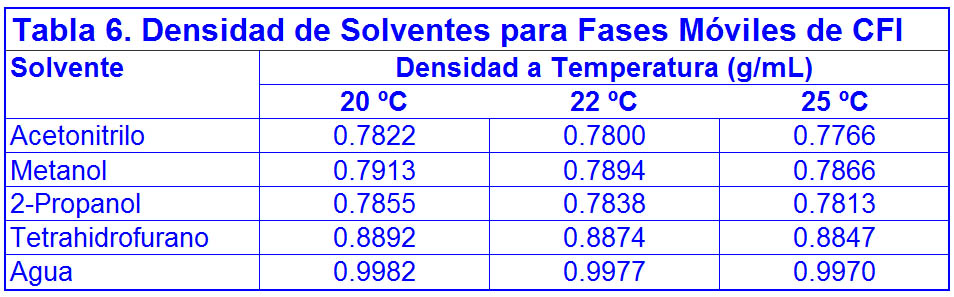
La TABLA 6 muestra la densidad para algunos solventes comunes, y permite la formulación de fases inversas por pesada de cada componente en la mezcla.
3. Seguridad
Los solvente usados generalmente en HPLC son muchas veces inflamables y moderadamente tóxicos, y por lo tanto han de almacenarse en una armario metálico de seguridad.
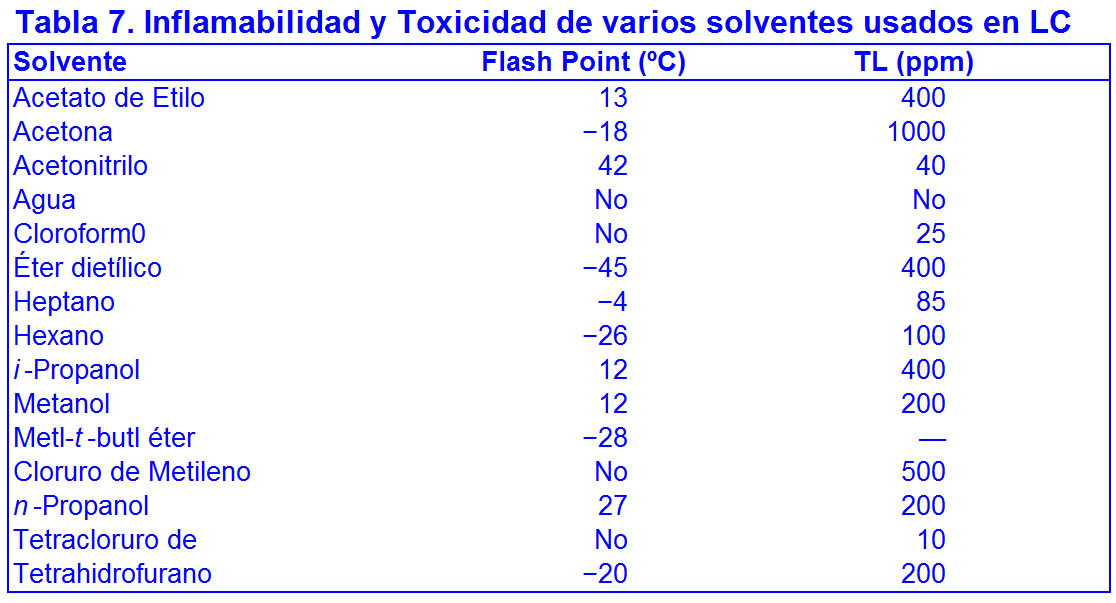
En la TABLA 7 se muestran los valores de Flash Point que indican la inflamabilidad del solvente. La experiencia indica que el metanol (FP 12 ºC) es moderadamente inflamable por lo que productos con FP por encima de ese valor no debería presentar ningún problema en términos de seguridad frente al fuego. Los solventes con FP inferiores son más peligrosos y deberían tratarse con la cautela adecuada.
Por cuanto respecta a la toxicidad los solventes deberían manipularse en campana exceptuando el agua. La indicación de su toxicidad viene dada el valor LD50 que es la cantidad en mg/Kg de cuerpo que causa un 50% de mortandad de la población. Sin embargo los solventes usados en el laboratorio muy raramente se ingestan y su peligro más inmediato es por contacto o inhalación. La Acetona con un LD50 no es claramente un problema aunque su FP de -18ºC requiere atención por cuanto respecta al riesgo de fuego.

