1. Desarrollar una Estrategia Previa
Los Métodos de Purificación en Cromatografía FLASH, y especialmente en UPFP (Ultra Performance Flash Purification) se desarrollan, o deberían desarrollarse, con los datos obtenidos en separaciones previas en Cromatografía de Capa Fina (TLC) y seguir los pasos siguientes:
- Generar una mezcla binara que permita que los compuestos de interés estén comprendidos entre Rf 0.15 y Rf 0.35 para una separación óptima
- Optimizar la separación modificando la fuerza y/o la selectividad del eluyente
- Aumentar la velocidad transformando un método Isocrático a Gradiente
Normalmente los datos generados en TLC se expresan en términos de Retención (Rf) que se mide por la relación entre la distancia recorrida por el compuesto y el frente del solvente, mientras que en purificaciones en columna se mide la retención en función de Volumen de Columna (CV) que generalmente se define como el volumen de solvente necesario para mover los componentes a lo largo de la columna.
La relación siguiente permite transferir los datos obtenidos en TLC a los términos usados en FLASH:
CV=1/Rf
De esta relación se deduce que un valor de Rf menor corresponde a un mayor valor de CV que, a su vez, indica un mayor tiempo de interacción entre el compuesto de interés y el material del lecho de la columna.
Una vez obtenida una separación adecuada (los compuestos de interés han de estar comprendidos entre Rf 0.15 y Rf 0.35 para una separación óptima) es posible trasponer un método desarrollado en TLC y en condiciones isocráticas a un método UPFP en condiciones de gradiente.
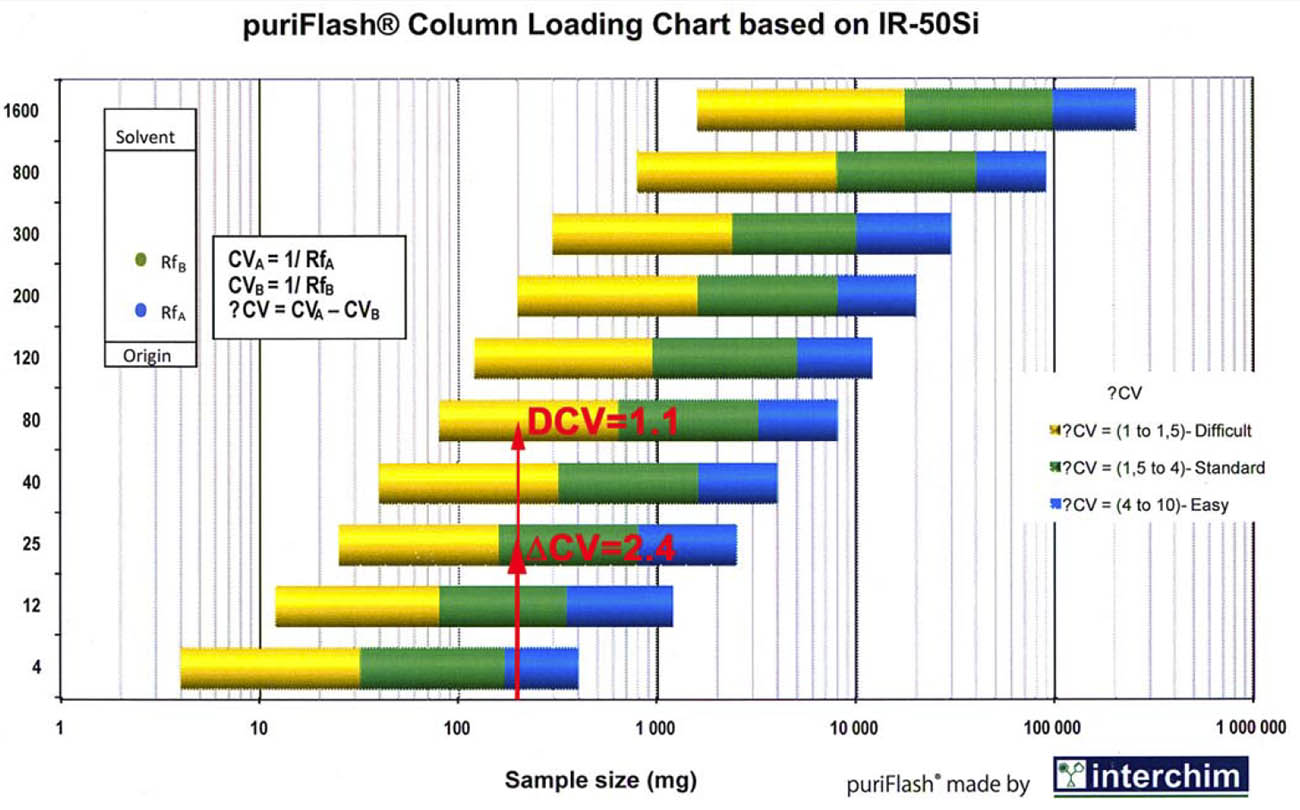
Supongamos los casos siguientes de la Figura 1:
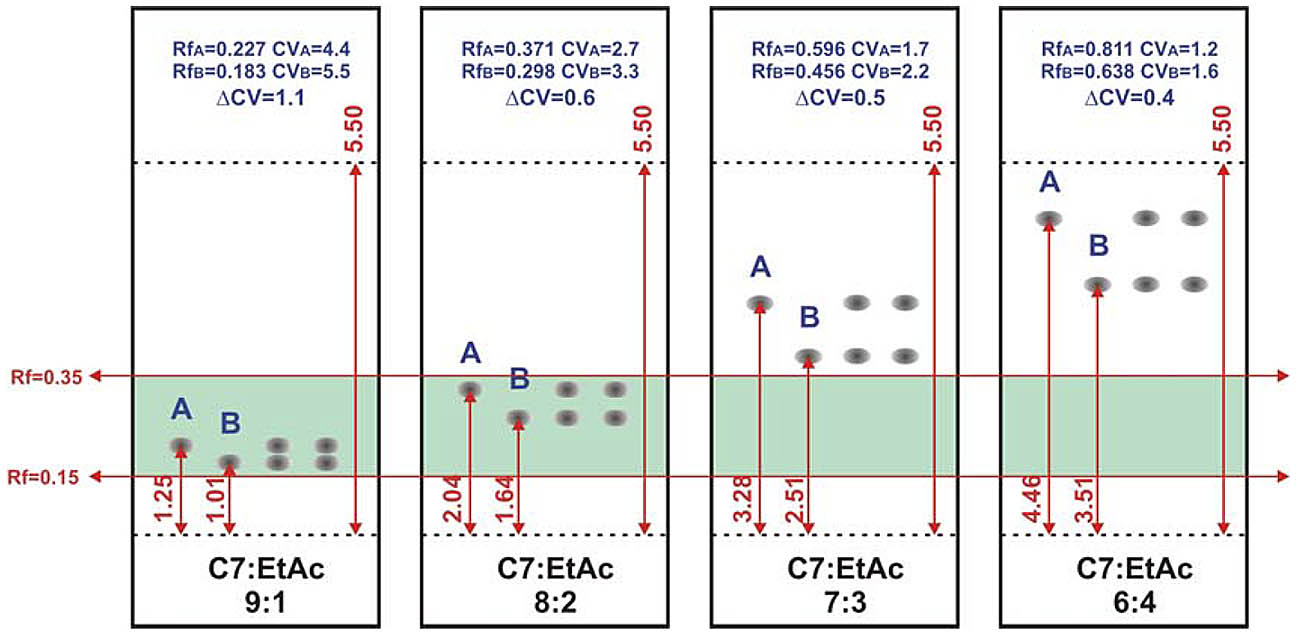
- Caso 1. Heptano:Acetato de Etilo 9:1. Compuestos de interés en el intervalo Rf entre 0.15 y 0.35. RfA=1.25/5.50=0.227, CVA=1/0.227= 4.4. RfB=1.01/5.50=0.183, CVB=1/0.227= 5.5. ΔCV=5.5-4.4=1.1
- Caso 2. Heptano:Acetato de Etilo 8:2. Compuestos de interés en el intervalo Rf entre 0.15 y 0.35. RfA=2.04/5.50=0.371, CVA=1/0.371= 2.7. RfB=1.64/5.50=0.298, CVB=1/0.298= 3.3. ΔCV=3.3-2.7=0.6
- Caso 3. Heptano:Acetato de Etilo 7:3. Compuestos de interés fuera del intervalo Rf entre 0.15 y 0.35. RfA=3.28/5.50=0.596, CVA=1/0.596= 1.7. RfB=2.51/5.50=0.456, CVB=1/0.456= 2.2. ΔCV=2.2-1.7=0.5
- Caso 4. Heptano:Acetato de Etilo 6:4. Compuestos de interés fuera del intervalo Rf entre 0.15 y 0.35. RfA=4.46/5.50=0.811, CVA=1/0.811= 1.2. RfB=3.51/5.50=0.638, CVB=1/0.638= 1.6. ΔCV=1.6-1.2=0.4
Los cromatogramas en FLASH, con los eluyentes aplicados en las TLC, se muestran en la Figura 2:
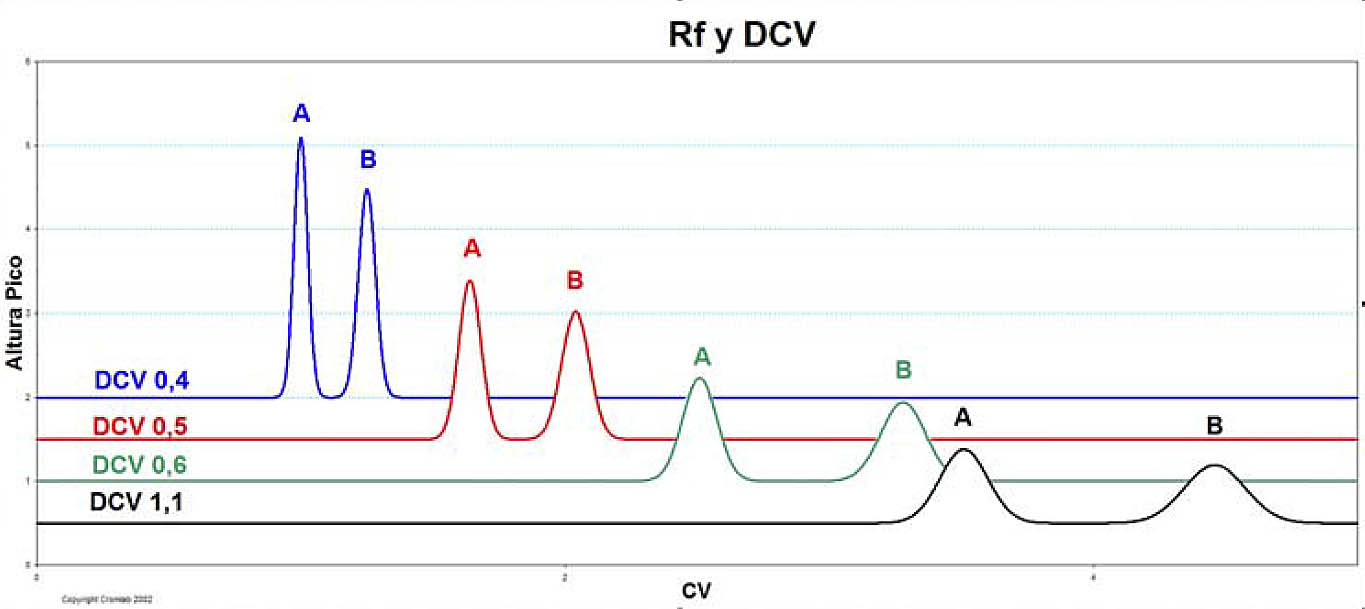
Una separación con ΔCV alto indica una mejor separación en UPFP o, como alternativa, una superior capacidad de carga.
Este otro ejemplo ilustra como conviene operar con un ΔCV alto:
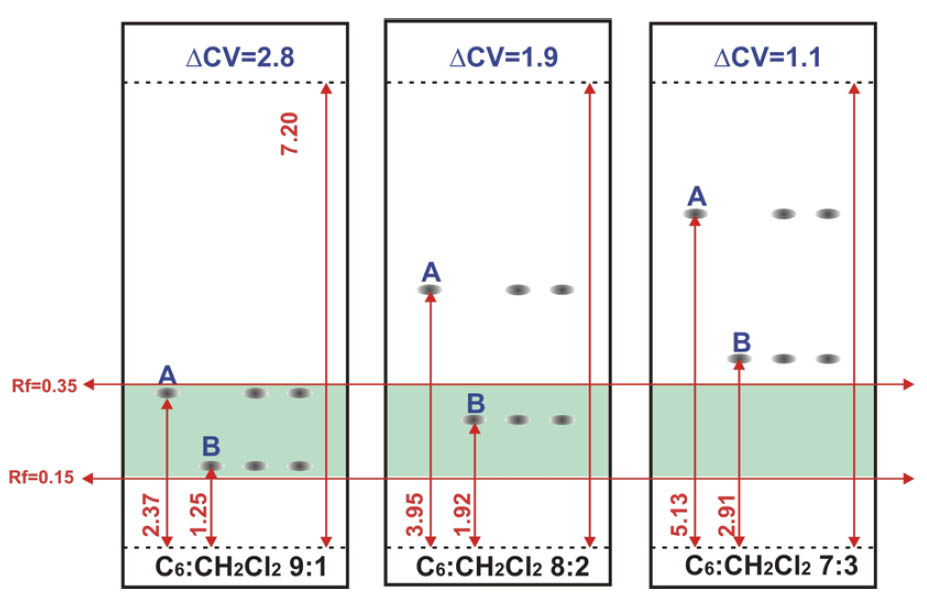
En las TLC’s anteriores (Figuras 3 y 4) se puede constatar que una separación con ΔCV de 2.8 permite, para una carga de 200 mg de crudo, usar una columna de 25g, mientras que para un ΔCV de 1.1, la columna necesaria pasa a ser de 80g.
2. Modificar Fuerza del Eluyente: un concepto básico muy útil en FLASH
Si la modificación de la concentración de los componentes de una mezcla binaria no logra el objetivo de obtener una separación de los componentes de un crudo en el intervalo entre Rf 0.15 y Rf 0.35 usar otros eluyentes con fuerza similar para modificar la selectividad puede ser el camino a seguir.
La Figura 5 muestra el llamado “Triángulo de Selectividad”. Este gráfico permite al técnico conseguir un cambio en la selectividad del solvente de un modo mucho más rápido que con una selección aleatoria.

La Tabla 1 muestra las características principales de los eluyentes usados en UPFP y el grupo al que pertenecen. En la tabla se especifican las longitudes de onda aproximadas en nm, por debajo de las cuales la absorbancia del solvente puede resultar inaceptable.
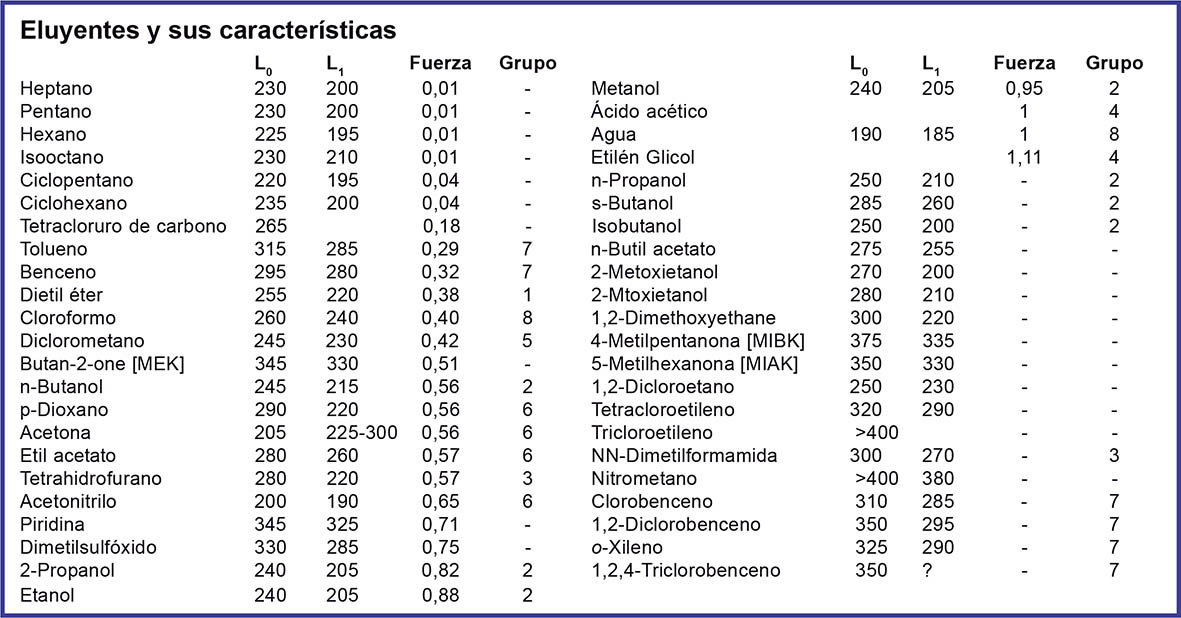
En trabajos cuantitativos la longitud de onda (L0) puede fijarse de tal manera que el valor de la absorbancia en una celda de 10mm sea 0.05 UA (relativa al agua, A1cm>0.05). En trabajos cualitativos, se puede trabajar a longitudes significativamente menores y la mayoría de los técnicos aceptan un valor de corte basado en 1UA (L1, relativa al agua, A1cm>1.0). Sin embargo si la curva de absorción sube fuertemente, puede que el rango de longitudes de onda disponibles no sea muy amplio.
Como ejemplo tomemos las placa siguientes, Figuras 6 y 7 , donde
A = Producto A, B = Producto A, C = CRUDO, A+B: Mix A+B:
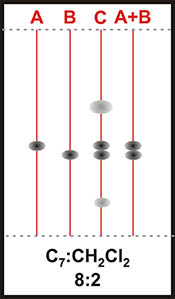
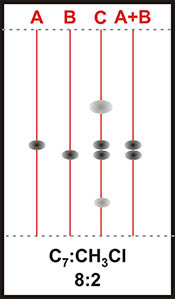
La separación de la Figura 6 se ha obtenido en SiO2 con Heptano:CH2Cl2 8:2. En estas condiciones la Fuerza del eluyente se calcula según:
FT = A x FA+B x FB
FT = 0.8 x 0.01+0.2 x 0.42 = 0.092
Donde:
- FT= Fuerza Total
- A=% A
- FA= Fuerza A (Heptano 0.01)
- B=%B
- FB= Fuerza B (Cloruro de Metileno 0.42)
El Triángulo de Selectividad de la Figura 5, indica que el Cloruro de Metileno (el más polar) pertenece al Grupo 5, y se tendrá que seleccionar un eluyente lo más alejado posible de ése Grupo, por ejemplo alguno del Grupo 2 o Grupo 8.
Si, por razones de estabilidad seleccionamos el Cloroformo, perteneciente al Grupo 8. la composición del nuevo eluyente binario (manteniendo el Heptano) será:
Bnuevo = B x FB/Fnuevo
y Bnuevo = 0.2 x 0.42/0.40 = 0.21
es decir una mezcla binaria de fuerza similar a la anterior con Cloruro de Metileno será también 8:2 (C7:CHCl3). La selectividad diferente mejora ligeramente la separación (ver Figura 7).
Si Seleccionamos, por ejemplo, el IPA (2-Propanol), del Grupo 2 para obtener una selectividad muy diferente pero con la misma fuerza eluyente resulta:
Bnuevo = B x FB/Fnuevo
y Bnuevo = 0.2 x 0.42/0.82 = 0.1
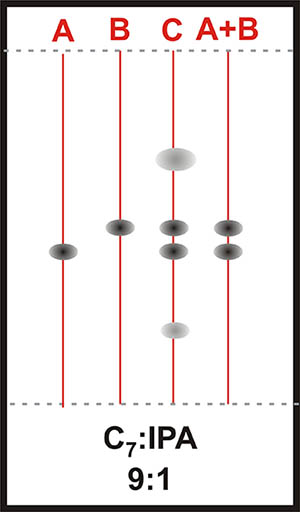
es decir es decir una mezcla binaria de fuerza similar a las anteriores con Cloruro de Metileno o Cloroformo ha de ser 9:1 (C7:IPA).
En este caso, la nueva selectividad invierte A y B pero se obtiene mejor separación (Ver Figura 8).
3. Usar un Gradiente para aumentar la velocidad
En general se usa una primera aproximación como la mostrada en la Figura 9:
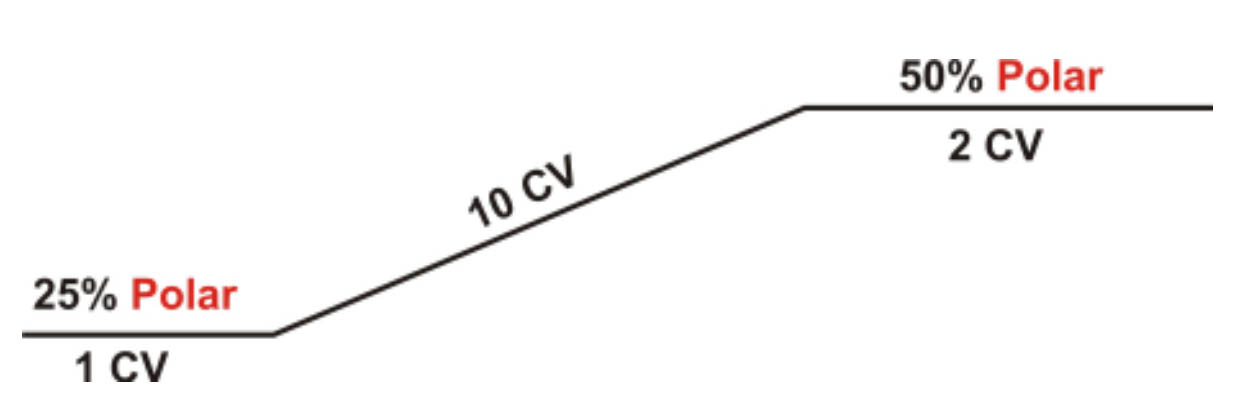
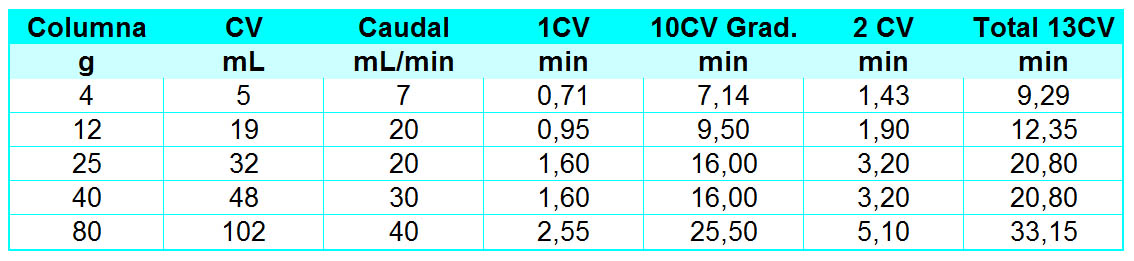
La Tabla2 muestra la transposición de CV a RT para varias columnas FLASH desde 4 a 80g de SiO2.